گلیکوزامینوگلیکان ها - هتروپلی ساکاریدهای با بار منفی خطی. قبلاً آنها را موکوپلی ساکارید می نامیدند، زیرا در ترشحات مخاطی (مخاط) یافت می شدند و به این ترشحات خاصیت چسبناک و روان کنندگی می دادند. این ویژگی ها به این دلیل است که گلیکوزامینوگلیکان ها می توانند مقادیر زیادی آب را به هم متصل کنند، در نتیجه ماده بین سلولی یک ویژگی ژله مانند به دست می آورد.
پروتئوگلیکان ها - ترکیبات مولکولی بالا متشکل از پروتئین (5-10٪) و گلیکوزامینوگلیکان (90-95٪). آنها ماده اصلی ماتریکس بین سلولی بافت همبند را تشکیل می دهند و می توانند تا 30٪ از جرم خشک بافت را تشکیل دهند.
پروتئین های موجود در پروتئوگلیکان ها با یک زنجیره پلی پپتیدی با وزن های مولکولی متفاوت نشان داده می شوند. اجزای پلی ساکارید پروتئوگلیکان های مختلف متفاوت است. پروتئوگلیکان ها از گروه بزرگی از پروتئین ها به نام متمایز هستند گلیکوپروتئین هااین پروتئین ها همچنین حاوی زنجیره های الیگوساکاریدی با طول های مختلف هستند که به صورت کووالانسی به ستون فقرات پلی پپتیدی متصل شده اند. جزء کربوهیدراتی گلیکوپروتئین ها از نظر جرم بسیار کوچکتر از پروتئوگلیکان ها است و بیش از 40 درصد جرم کل نیست. گلیکوپروتئین ها عملکردهای متفاوتی را در بدن انسان انجام می دهند و در تمام کلاس های پروتئین ها وجود دارند - آنزیم ها، هورمون ها، حمل و نقل، پروتئین های ساختاری، و غیره. -هورمون محرک گلیکوزامینوگلیکان ها و پروتئوگلیکان ها که اجزای ضروری ماتریکس بین سلولی هستند، نقش مهمی در فعل و انفعالات بین سلولی، تشکیل و حفظ شکل سلول ها و اندام ها و تشکیل داربست در طول تشکیل بافت دارند. پروتئوگلیکان ها و گلیکوزآمینوگلیکان ها با توجه به ویژگی های ساختار و خواص فیزیکوشیمیایی خود می توانند وظایف زیر را در بدن انسان انجام دهند:
آنها اجزای ساختاری ماتریکس خارج سلولی هستند.
پروتئوگلیکان ها و گلیکوزآمینوگلیکان ها به طور خاص با کلاژن، الاستین، فیبرونکتین، لامینین و سایر پروتئین های ماتریکس خارج سلولی تعامل دارند.
همه پروتئوگلیکان ها و گلیکوزآمینوگلیکان ها، که پلی آنیون هستند، می توانند علاوه بر آب، مقادیر زیادی کاتیون (Na + , K + ، Ca 2 + ) را متصل کرده و در نتیجه در تشکیل تورگور بافت های مختلف شرکت کنند.
پروتئوگلیکان ها و گلیکوزآمینوگلیکان ها نقش یک غربال مولکولی را در ماتریکس خارج سلولی بازی می کنند، آنها از گسترش میکروارگانیسم های بیماری زا جلوگیری می کنند.
اسید هیالورونیک و پروتئوگلیکان ها عملکرد فنری را در غضروف مفصلی انجام می دهند.
پروتئوگلیکان های حاوی سولفات هپاران به ایجاد یک سد فیلتراسیون در کلیه ها کمک می کند.
سولفات های کراتان و سولفات های درماتان شفافیت قرنیه را فراهم می کنند.
هپارین - ضد انعقاد؛
سولفات های هپاران اجزایی از غشای پلاسمایی سلول ها هستند، جایی که می توانند به عنوان گیرنده عمل کنند و در چسبندگی سلولی و تعاملات بین سلولی شرکت کنند. آنها همچنین به عنوان اجزای سیناپسی و سایر وزیکول ها عمل می کنند.
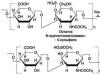
ساختار و کلاس های گلیکوزآمینوگلیکات ها . گلیکوزامینوگلیکان ها زنجیره های بلند و بدون انشعاب از هتروپلیس-کاریدها هستند. آنها از تکرار واحدهای دی ساکارید ساخته شده اند. یکی از مونومرهای این دی ساکارید هگزورونیک اسید (D-glucuronic acid یا L-iduronic acid) است و مونومر دوم یک مشتق از آمینو قند (گلوکز یا گالاکتوزامین) است. قندهای آمینه NH 2 -rpynna معمولاً استیله می شوند که منجر به ناپدید شدن بار مثبت ذاتی آنها می شود. علاوه بر اسید هیالورونیک، تمام گلیکوزامینوگلیکان ها حاوی گروه های سولفات به شکل O-استرها یا N-سولفات هستند.
اسید هیالورونیک در بسیاری از اندام ها و بافت ها یافت می شود. در غضروف با پروتئین همراه است و در تشکیل تجمعات پروتئوگلیکان شرکت می کند؛ در برخی از اندام ها (بدن زجاجیه چشم، بند ناف، مایع مفصلی) به صورت آزاد نیز یافت می شود. فرض بر این است که اسید هیالورونیک در مایع مفصلی به عنوان روان کننده عمل می کند و اصطکاک بین سطوح مفصلی را کاهش می دهد. واحد دی ساکارید تکرار شونده در اسید هیالورونیک دارای ساختار زیر است:
اسید هیالورونیک حاوی چندین هزار واحد دی ساکارید است، وزن مولکولی آن به 10 5 - 10 7 D می رسد.
کندرویتین سولفات - رایج ترین گلیکوزامینوگلیکان ها در بدن انسان؛ آنها در غضروف، پوست، تاندون ها، رباط ها، شریان ها و قرنیه چشم یافت می شوند. کندرویتین سولفات ها جزء مهم آگرکان، پروتئوگلیکان اصلی ماتریکس غضروف هستند. در بدن انسان، 2 نوع کندرویتین سولفات وجود دارد: کندرویتین-4-سولفات و کندرویتین-6-سولفات. آنها به همین ترتیب ساخته می شوند، تفاوت فقط به موقعیت گروه سولفات در مولکول N-acetylgalactosamine مربوط می شود.

یک زنجیره پلی ساکارید از کندرویتین سولفات حاوی حدود 40 واحد دی ساکارید تکرار شونده است و دارای وزن مولکولی 10 4 - 10 6 D است.
سولفات کراتان - ناهمگن ترین گلیکوزامینوگلیکان ها؛ از نظر محتوای کل کربوهیدرات ها و توزیع در بافت های مختلف با یکدیگر متفاوت هستند. سولفات کراتان I در قرنیه چشم قرار دارد و علاوه بر واحد دی ساکارید تکرار شونده، L-fucose، D-mannose و اسید سیالیک دارد. کراتان سولفات II در غضروف، استخوان ها و دیسک های بین مهره ای یافت شده است. علاوه بر قندهای واحد دی ساکارید، حاوی N-acetylgalactosamine، L-fucose، D-mannose و اسید سیالیک است. کراتان سولفات II بخشی از آگرکان و برخی پروتئوگلیکان های کوچک ماتریکس غضروف است. برخلاف سایر گلیکوزامینوگلیکان ها، کراتان سولفات ها به جای اسید هگزورونیک حاوی گالاکتوز هستند.

وزن مولکولی یک زنجیره سولفات کراتان از 4 × 10 3 تا 20 × 10 3 D است.
سولفات درماتان این به طور گسترده در بافت های حیوانی، به ویژه در پوست، رگ های خونی و دریچه های قلب توزیع می شود. درماتان سولفات به عنوان بخشی از پروتئوگلیکان های کوچک (بیگلیکان و دکورین)، در ماده بین سلولی غضروف، دیسک های بین مهره ای و منیسک ها یافت می شود. واحد دی ساکارید تکرار شونده درماتان سولفات دارای ساختار زیر است.

وزن مولکولی یک زنجیره سولفات درماتان از 15 × 10 3 تا 40 × 10 3 D است.
هپارین - یک جزء مهم از سیستم خون ضد انعقاد (به عنوان یک ضد انعقاد در درمان ترومبوز استفاده می شود). توسط ماست سل ها سنتز می شود و در گرانول های درون این سلول ها یافت می شود. بیشترین مقدار هپارین در ریه ها، کبد و پوست یافت می شود. واحد دی ساکارید هپارین مشابه واحد دی ساکارید هپاران سولفات است. تفاوت بین این گلیکوزامینوگلیکان ها در این است که هپارین دارای گروه های N-سولفات بیشتری است و هپاران سولفات دارای گروه های N-استیل بیشتری است. وزن مولکولی هپارین از 6 × 10 3 تا 25 × 10 3 D است.

هپاران سولفات در بسیاری از اندام ها و بافت ها یافت می شود. بخشی از پروتئوگلیکان های غشای پایه است. هپاران سولفات یک جزء ثابت از سطح سلول است. ساختار واحد دی ساکارید هپاران سولفات مانند هپارین است. وزن مولکولی زنجیره سولفات هپاران از 5 × 10 3 تا 12 × 10 3 D است.
ساختار و انواع پروتئوگلیکان ها . ماتریکس خارج سلولی حاوی پروتئوگلیکان های مختلف است. در میان آنها موارد بسیار بزرگ وجود دارد - به عنوان مثال، agrecan و versican. علاوه بر آنها، ماتریکس خارج سلولی حاوی مجموعه کاملی از به اصطلاح پروتئوگلیکان های کوچک است که به طور گسترده در انواع مختلف بافت همبند توزیع شده و عملکردهای متنوعی را در آنجا انجام می دهند. پروتئوگلیکان اصلی ماتریکس غضروف نامیده می شود آگرکان، 10 درصد وزن بافت اصلی و 25 درصد وزن خشک ماتریکس غضروف است. این یک مولکول بسیار بزرگ است که در آن تا 100 زنجیره سولفات کندرویتین و حدود 30 زنجیره سولفات کراتان به یک زنجیره پلی پپتیدی متصل است. شکل مولکول آگرکان شبیه یک برس بطری است. در بافت غضروفی، مولکولهای آگرکان با اسید هاالورونیک و یک پروتئین اتصال کوچک به تودههایی ترکیب میشوند. هر دو جزء با پیوندهای غیرکووالانسی در ناحیه دامنه G1 به آگرکان متصل می شوند. دامنه G 1 با تقریباً پنج واحد دی ساکارید اسید هیالورونیک برهمکنش میکند، سپس این کمپلکس توسط یک پروتئین اتصال تثبیت میشود. دامنه G 1 و پروتئین اتصال با هم 25 واحد دی ساکارید اسید هیالورونیک را اشغال می کنند. سنگدانه نهایی با وزن مولکولی بیش از 200 × 10 6 D از یک مولکول اسید هیالورونیک و 100 مولکول آگرکان (و همان مقدار پروتئین اتصال دهنده) تشکیل شده است. هماهنگی مونتاژ این توده ها یک عملکرد مرکزی سلول های غضروفی است. آگرکان و پروتئین اتصال به مقدار لازم توسط این سلول ها تولید می شود. این اجزا می توانند در داخل سلول با یکدیگر تعامل داشته باشند، اما فرآیند تجمع در ماتریکس خارج سلولی به طور کامل تکمیل می شود. نشان داده شده است که اسید هیالورونیک بر روی سطح کندروسیت ها توسط یک سنتتاز خاص تشکیل می شود و به فضای بین سلولی "رانده می شود" تا با آگرکان و پروتئین اتصال دهنده متصل شود. بلوغ یک مجتمع سه تایی فعال عملکردی حدود 24 ساعت است.
پروتئوگلیکان های کوچک پروتئوگلیکان های کوچک پروتئوگلیکان هایی با وزن مولکولی کم هستند. آنها در غضروف، تاندون ها، رباط ها، منیسک ها، پوست و سایر انواع بافت همبند یافت می شوند. این پروتئوگلیکان ها دارای یک پروتئین هسته کوچک هستند که یک یا دو زنجیره گلیکوزامینوگلیکان به آن متصل است. بیشترین مطالعه شده عبارتند از دکورین، بیگلیکان، فیبرومودولین، لومیکان، پرلکان. پروتئین های اصلی بیگلیکان و دکورین از نظر اندازه و ساختار مشابه هستند (به ترتیب وزن مولکولی 36000 و 38000 D). آنها چندین تکرار پشت سر هم غنی از لوسین دارند که ساختارهای α-مارپیچ یا β-ساختار را تشکیل می دهند. در انتهای N و C این پروتئین ها، دامنه هایی حاوی پیوندهای S-S وجود دارد. پروتئین های هسته به طور قابل توجهی در ساختار اولیه خود در نواحی ترمینال N تفاوت دارند، که تفاوت در اتصال گلیکوزامینوگلیکان ها را تعیین می کند. بیگلیکان حاوی یک سری در موقعیت های 5 و 11 است که اتصال دو زنجیره پلی ساکارید را تضمین می کند. دکورین حاوی یک سری در موقعیت است. 4، بنابراین به یک زنجیره پلی ساکارید می پیوندد در این پروتئوگلیکان ها، زنجیره های پلی ساکارید با سولفات درماتان با وزن مولکولی ~ 30000 D نشان داده می شود. حاوی سرین است، اما دارای چندین باقی مانده تیروزین سولفاته است، بنابراین یک یا دو زنجیره سولفات کراتان به آن متصل می شود. پروتئین هسته فیبرومودولین نه در ترمینال N، بلکه در ناحیه غنی از لوسین، از طریق گروه NH 2 آسپاراژین. پروتئوگلیکان های کوچک ماکرومولکول های چند منظوره هستند. آنها می توانند به سایر اجزای بافت همبند متصل شوند و بر ساختار و عملکرد آنها تأثیر بگذارند. به عنوان مثال، دکورین و فیبرومودولین به فیبرهای کلاژن نوع II متصل می شوند و قطر آنها را محدود می کنند (یعنی از تشکیل فیبریل های ضخیم جلوگیری می کنند). دکورین و بیگلیکان وقتی به فیبرونکتین متصل می شوند، چسبندگی سلولی را مهار می کنند و هنگامی که به فاکتور رشد تومور متصل می شوند، فعالیت میتوژنیک آن را کاهش می دهند. توسعه و ترمیم بافت همبند.
CANINA Pharma داروهایی را برای پیشگیری و درمان آرتروپاتی تولید می کند.
ویتامین CANINA قابل سفارش است
آرتروپاتی(از یونانی. arthron-joint و pathos-suffering)، تغییر تغذیه ای در مفصل می تواند هم در سگ های بالغ و هم در توله سگ های نژادهای متوسط، بزرگ و غول پیکر ایجاد شود. توله های این نژادها به سرعت رشد می کنند و خیلی زود به اندازه سگ های بزرگ می رسند، اما این بی خطر نیست. اختلالات رشد و تشکیل اسکلت - مانند دیسپلازی هیپ، استئوکندریت تشریح کننده، انحنای شعاع، استئودیستروفی هیپرتروفیک - بیماری های شایع مرتبط با رشد حیوان هستند. در سگ های بالغ، آسیب های تروماتیک مفاصل، ضعف دستگاه رباط، بیماری های دژنراتیو مفصلی که یک مورد خاص آن آرتروز است، شایع است.
آرتروز- یک بیماری گسترده دژنراتیو دیستروفیک مفاصل که علت آن آسیب به بافت غضروفی سطوح مفصلی و همچنین استخوان زیر غضروفی، رباط ها، کپسول، غشای سینوویال و عضلات اطراف مفصلی تا تغییر شکل کامل مفصل است. و عملکرد آن به طور جزئی یا کامل از بین می رود. استئوآرتریت نتیجه عوامل مکانیکی و بیولوژیکی است که تشکیل غضروف مفصلی و سلول های استخوان زیر غضروفی را مختل می کند. این می تواند توسط عوامل بسیاری از جمله ژنتیکی، تکاملی، متابولیک و تروماتیک آغاز شود. استئوآرتریت مبتنی بر تغییرات پاتولوژیک است که در نتیجه اختلال در فرآیندهای طبیعی سنتز و تخریب در سلولهای غضروفی و ماتریکس غضروف مفصلی و استخوان ساب غضروفی رخ میدهد.
شایع ترین علائم آرتروز: لنگش مداوم. مشکل برخاستن و واکنش درد مزمن. لنگش با واکنش درد در مفاصل و محدودیت دامنه حرکتی اندام ها همراه است. این می تواند پیشرفت کند و همچنین به طور ناگهانی به دلیل آسیب جزئی یا در طول ورزش شدید ظاهر شود.
20 درصد از سگ های بالای 1 سال از آرتروز رنج می برند. بیش از 95 درصد موارد آرتروز در سگ های بالای 5 سال رخ می دهد. لنگش یک انگیزه رایج برای مراجعه به دامپزشک است.
عوامل خطر برای ایجاد آرتروز
1. سن
بین 8 تا 13 سالگی، بیش از نیمی از سگ ها از آرتروز رنج می برند.
سایز 2:
· 45 درصد از سگ های مبتلا به استئوآرتریت بزرگ هستند و نژادهای غول پیکر پیشرو هستند (بیش از نیمی از موارد).
· 28 درصد موارد استئوآرتریت در سگ های با جثه متوسط رخ می دهد.
27 درصد مربوط به نژادهای سگ کوچک است.
3. چاقی
4. آسیب های استخوانی
جراحی روی مفاصل باعث ایجاد آرتروز می شود.
5. افزایش فعالیت
6. بخصوص در دوره رشد.
امروزه هم در دارودرمانی دامپزشکی و هم در داروسازی پزشکی، از داروهای مختلف بر پایه گلیکوزآمینوگلیکان ها برای درمان و پیشگیری از آرتروپاتی و دیسکوپاتی ("فتق دیسک") استفاده می شود. منبع تولید آنها موادی با منشاء حیوانی و گیاهی (معده مرغ، خروس، نرم تن، جلبک و غیره) است.
گلیکوزامینوگلیکان ها (GAGs)
- اینها مولکولهای پلی ساکاریدی بلند و بدون انشعاب هستند که عمدتاً از کمپلکس های دی ساکاریدی تکرار شونده تشکیل شده اند. آنها توسط قندهای آمینه (D-گالاکتوزامین وD-گلوکوزامین)، معمولاً شامل اسید اورونیک است.
به دلیل فراوانی سولفات و همچنین گروه های کربوکسیل اسید اورونیک، GAG ها پلی آنیون هستند و دارای بار منفی هستند که به آنها اجازه می دهد به پروتئین ها و لیپیدها متصل شوند. این ماده پروتئوگلیکان ها و گلیکولیپیدها را تولید می کند. این بار منفی است که خواص فیزیکوشیمیایی GAG ها را تعیین می کند مانند ویسکوزیته بالا و مقاومت در برابر فشار، که به ویژه برای اجزای غضروف مفصلی، مایع مفصلی و سایر عناصر سیستم اسکلتی عضلانی مهم است. از سوی دیگر، تعامل آنها با ماکرومولکول های خارج سلولی، پروتئین ها و اجزای سطح سلولی، سازماندهی ساختاری ماتریکس بافت همبند را تضمین می کند.
GAGهایی که بیشترین اهمیت فیزیولوژیکی را دارند عبارتند از هیالورونیک اسید، کندرویتین سولفات، کراتان سولفات، هپارین، هپاران سولفات و درماتان سولفات.
GAG ها در اجرای تعداد زیادی از فرآیندهای حیاتی نقش دارند و بخشی از بافت های مختلف هستند. بنابراین، هپارین از گرانول های ماست سل آزاد می شود و یک ضد انعقاد است. شواهدی در ادبیات وجود دارد که بر وضعیت عملکردی لنفوسیت های T و B تأثیر می گذارد. مقاومت بافت ها را در برابر هیپوکسی افزایش می دهد، فاز هوازی متابولیسم را تحریک می کند، پراکسیداسیون و فعالیت هیدرولازهای لیزوزومی و نفوذپذیری دیواره عروقی را کاهش می دهد. سولفات هپاران نقش یک محافظ درون زا از اندوتلیوم عروقی را ایفا می کند. سولفات درماتان تا حد زیادی ساختار پوست، رگ های خونی و دریچه های قلب را تعیین می کند. سولفات کراتان در ساختار قرنیه، بافت همبند شل، اسکلت گنجانده شده است. اسید هیالورونیک و کندرویتین سولفات عمدتاً در مفاصل یافت می شوند. علاوه بر این، این اجزا در تاندون ها، دیسک های مهره ای، قرنیه، اندوکارد، پلور و صفاق قرار دارند. بسیاری از بیماریهای تعیینشده ژنتیکی وجود دارند که با نقص در شکلگیری و متابولیسم سلولهای GAG مرتبط با غشاء همراه هستند.
با توجه به نقش GAG به عنوان یک داروی ارتومولکولی در پیشگیری و درمان بیماری های مفصلی، برای بهترین نتیجه، داروهای حاوی GAG باید روزانه مصرف شوند و در دوره های طولانی (از 45 تا 90 روز بسته به شدت مفصل) مصرف شوند. خسارت). اثر درمانی پس از مصرف یک دوره داروی حاوی GAG برای 6-12 ماه باقی می ماند. برای جلوگیری از بی اعتبار شدن چنین ماده ارزشمندی مانند GAG، لازم است دوزهای توصیه شده را رعایت کنید. با این حال، با چاقی، مصرف دیورتیک ها، دوز باید افزایش یابد. و در صورت وجود یک فرآیند التهابی در دستگاه گوارش، استفاده از داروهای حاوی GAG همراه با غذا ضروری است. داروهای غضروفی خوراکی بدون شک برای درمان طولانی مدت نسبت به انواع تزریقی ارجحیت دارند.
در مقایسه داروهای حاوی GAG با داروهای ضد التهابی غیر استروئیدی که فقط به طور موقت درد را تسکین می دهند، می توان به عدم وجود عوارض جانبی جدی (آسیب به کبد و دستگاه گوارش) اشاره کرد.
از آنجایی که بافت های مفصل دارای انعطاف پذیری انطباقی بالایی هستند، استفاده از داروهای حاوی GAG در طول دوره توانبخشی پس از آرتریت سپتیک و به عنوان یک درمان کمکی در مرحله حاد دوره آنها تأثیر مثبت قابل توجهی می دهد.
نظارت بر مصرف GAGs به عنوان بخشی از غضروف محافظ در حیوانات پیر بسیار مهم است. در این دوره از زندگی، عملکرد کندروسیت ها برای سنتز کندرویتین-4-سولفات کاهش می یابد و این جزء با عناصر دیگر با بدتر شدن ویژگی های کیفی بافت غضروف جایگزین می شود. کندرویتین-4-سولفات نیز تأثیر مثبتی بر سیستم قلبی عروقی دارد. این ماده توسط پلاکت ها آزاد می شود و در تنظیم انعقاد خون نقش دارد و از تشکیل لخته های خونی که باعث اختلالات میکروسیرکولاسیون در بافت ها می شود، جلوگیری می کند. بنابراین، انتصاب غضروف محافظ به شما امکان می دهد مشکلات مربوط به اختلال در فعالیت عملکردی سیستم اسکلتی عضلانی و سایر سیستم های بدن را در این دوره سنی کاهش دهید. این شرایط متابولیک مطلوبی را برای ترمیم سلول ها تحت تأثیر عوامل نامطلوب ایجاد می کند. این در مورد حیوانات در حال رشد، زمانی که سنتز شدید غضروف وجود دارد، و همچنین در آسیب شناسی مربوط به سن، زمانی که تشکیل اجزای غضروف کاهش می یابد، صادق است.
همراه با استفاده موفقیت آمیز از داروهای حاوی GAG در درمان پاتولوژی های مفصلی، اخیراً گلیکوزامینوگلیکان در غدد درون ریز کاربرد پیدا کرده است، یعنی در درمان نفروپاتی دیابتی، که یک عارضه هولناک دیابت شیرین است. تا همین اواخر، تنها عامل بیماری زا قادر به از بین بردن فشار خون داخل گلومرولی، یعنی. برای تأثیرگذاری بر مکانیسم اصلی ایجاد آسیب کلیه، مهارکنندههای آنزیم مبدل آنژیوتانسین (ACE) در نظر گرفته شد. هیپرگلیسمی باعث نقض ساختار غشای پایه گلومرول کلیه می شود که با کاهش سنتز اجزای ساختاری اصلی - گلیکوزامینوگلیکان ها همراه است. این منجر به از دست دادن انتخاب بار غشای پایه می شود، در نتیجه مولکول های آلبومین به فیلتر کلیه نفوذ می کنند. برای بازیابی غشای پایه، توصیه می شود از آماده سازی های حاوی GAG استفاده کنید.
اثر محافظتی نفرو گلیکوزامینوگلیکان ها از جمله توانایی آنها در مهار اثرات فرآیندهای اسکلروتیک در کلیه ها، بازگرداندن تشکیل سولفات هپاران، مهمترین عنصر ساختاری غشای پایه کلیه ها مورد بحث قرار گرفته است.
ماده اولیه برای تولید فرآورده های حاوی GAG توسط متخصصان آلمانی نرم تنان Perna canaliculus بود. این نوعی صدف است که در سواحل نیوزلند صید شده است. مشاهده شده است که افرادی که این صدف ها را مصرف می کنند، تغییرات تخریبی و التهاب کمتری در مفاصل تجربه می کنند (اندرسون، 1999، وان اسکات، 1997). به طور سنتی، جمعیت Maiori برای قرن ها به طور منظم صدف می خورند. آنها بر خلاف جمعیت ساکن در بخش مرکزی این قلمرو، به میزان کمتری از آرتروز رنج می برند. این غذای دریایی حاوی غلظت بالایی از گلیکوزامینوگلیکان ها، کندرویتین سولفات و همچنین اسیدهای چرب ضروری امگا 3 و آنتی اکسیدان ها است.
در دفاع از هزینه بالای دارو نسبت به آنالوگ ها، می توان به بیوژنیسیته غیرقابل مقایسه بیشتر ماده فعال دارو در ساختارهای بافت همبند بدن حیوان اشاره کرد. یک مزیت مهم (Canina pharma GmbH) وجود تعداد بیشتری از مواد فعال در ترکیب آن است: اسید هیالورونیک، کندرویتین - 4 - سولفات، کندرویتین - 6 - سولفات، سولفات درماتان، سولفات کراتان، سولفات هپارین و سولفات هپاران. پس از 14 روز، یک اثر مثبت مشاهده می شود، اما مهم است که به یاد داشته باشید که تنها با استفاده سیستماتیک می توان یک اثر مثبت پایدار به دست آورد.
نتیجه گیری:
1. مواد مخدر، یا به دلیل این ترکیبات حاوی مقدار نامساوی ماده فعال هستند.
5. و جایگزینی برای استفاده از NSPS هستند.
6. GAG شامل مواد فعال بیولوژیکی لازم برای بازیابی ساختار غشای پایه کلیه در نفروپاتی دیابتی است.
7. عناصر اضافه شده به رژیم غذایی می توانند فرآیندهای التهابی دخیل در ایجاد آرتروز را تعدیل کنند. آنها همچنین باعث ترمیم غضروف سطح مفصل می شوند و از بدن در برابر استرس اکسیداتیو محافظت می کنند.
پروتئین های کربوهیدرات
دو زیر گروه از پروتئین های حاوی کربوهیدرات وجود دارد: پروتئوگلیکان ها و گلیکوپروتئین ها. تفاوت های قابل توجهی بین این زیر کلاس ها وجود دارد:
گلیکوپروتئین ها نقش ساختاری دارند
روش های اتصال کربوهیدرات به پروتئین
گلیکوپروتئین ها- پروتئین هایی که به عنوان یک گروه مصنوعی حاوی مقدار کمی کربوهیدرات (تا 15٪) هستند که توسط پیوندهای کووالانسی به رادیکال های اسید آمینه متصل شده اند. قسمت کربوهیدرات شامل هگزوزها (گالاکتوز، مانوز، به ندرت گلوکز)، پنتوزها (گزیلوز، آرابینوز)، دئوکسی قندها (فوکوز، رامنوز)، قندهای آمینه (استیل گالاکتوزامین، استیل گلوکوزامین)، نورآمینیک اسید و استرهای اسید استیک آن (اسیدهای سیالیک) است. آنها یا توسط یک پیوند N-گلیکوزیدی به نیتروژن آمید آسپاراژین، یا توسط یک پیوند O-گلیکوزیدی به گروه هیدروکسی یک باقیمانده سرین، ترئونین یا هیدروکسی لیزین متصل می شوند. بیشتر این پروتئین ها خاصیت کمی اسیدی دارند. در گروه گلیکوپروتئین ها، سروموکوئیدها (سروگلیکوئیدها) متمایز می شوند که دارای خواص اسیدی بارز بوده و در اسیدهای پرکلریک، تری کلرواستیک و سولفوسالیسیلیک محلول هستند. این بخش، که 1٪ از کل پروتئین های آب پنیر را تشکیل می دهد، شامل 12٪ از کل کربوهیدرات های پلاسما است.
عملکرد گلیکوپروتئین ها

طرح ساختار پروتئین گیرنده.
- ساختاری - دیواره سلولی باکتری، ماتریکس استخوان، به عنوان مثال، کلاژن، الاستین؛
- محافظ - به عنوان مثال، آنتی بادی ها، اینترفرون، فاکتورهای انعقاد خون (پرترومبین، فیبرینوژن).
- گیرنده - اتصال اثر منجر به تغییر در ساختار پروتئین گیرنده می شود که باعث پاسخ درون سلولی می شود.
- هورمون های هورمونی - گنادوتروپیک، آدرنوکورتیکوتروپ و هورمون های محرک تیروئید؛
- آنزیمی - کولین استراز، نوکلئاز؛
- انتقال - انتقال مواد در خون و از طریق غشاها، به عنوان مثال، ترانسفرین، ترانسکورتین، آلبومین، Na +، K + -ATPase.
پروتئوگلیکان ها
گروه دیگری از گلیکوکونژوگیت ها - پروتئوگلیکان ها - با حضور پلی ساکاریدهای بزرگ متشکل از بقایای دی ساکاریدهای تکراری مشخص می شود. اینها ترکیبات آبدوست هستند که شامل 20-80٪ کربوهیدرات است. اجزای کربوهیدرات پروتئوگلیکان ها گلیکوزآمینوگلیکان نامیده می شوند. 7 نوع گلیکوزامینوگلیکان وجود دارد که 5 نوع آن حاوی گلوکورونیک اسید است (اینها شامل اسید هیالورونیک، کندرویتین-4-سولفات و کندرویتین-6-سولفات، هپارین و هپاران سولفات)، نوع ششم (درماتان سولفات) حاوی ایدورونیک (گالاکتورونیک) است. اسید ، هفتمین (سولفات کراتان) - گالاکتوز. اسیدهای سیالیک، مانوز، زایلوز در حداقل مقدار وجود دارند. پروتئوگلیکان ها به دلیل وجود تعداد زیادی گروه کربوکسیل و باقی مانده های اسید سولفوریک دارای خواص اسیدی قوی هستند. دی ساکاریدها شامل هر اسید اورونیک و یک آمینو قند هستند. دی ساکاریدها که به طور مکرر تکرار می شوند، زنجیره های اولیگو و پلی ساکارید - گلیکان ها را تشکیل می دهند. برای بخش کربوهیدرات، نام های دیگری وجود دارد - هتروپلی ساکاریدهای اسیدی (از آنجایی که گروه های اسیدی زیادی دارند)، گلیکوزامینوگلیکان ها (حاوی گروه های آمینه). بیش از حد گروه های آنیونی (سولفات، کربوکسیل) به مولکول های گلیکوزامینوگلیکان بار منفی زیادی می دهد.

ساختار اسید هیالورونیک و کندرویتین سولفات.
نمایندگان اصلی گلیکوزامینوگلیکان های ساختاری اسید هیالورونیک، کندرویتین سولفات، کراتان سولفات و درماتان سولفات هستند. این مولکول ها بخشی از پروتئوگلیکان ها هستند که وظیفه آنها پر کردن فضای بین سلولی و حفظ آب در اینجا است، همچنین به عنوان یک جزء روان کننده و ساختاری مفاصل و سایر ساختارهای بافتی عمل می کنند.
بخش کربوهیدرات، مشابه گلیکوپروتئین ها، از طریق باقی مانده های سرین و آسپاراژین به پروتئین متصل می شود.

طرح ساختار پروتئوگلیکان های ماده بین سلولی.
عملکرد پروتئوگلیکان ها
از نظر عملکرد، پروتئوگلیکان های ساختاری برای فضای بین سلولی، به ویژه بافت همبند، که فیبرهای کلاژن در آن غوطه ور هستند، مهم هستند. با استفاده از میکروسکوپ الکترونی مشخص شد که آنها ساختار درختی دارند. مولکولهای گلیکان بسیار آبدوست هستند، یک ماتریکس ژلهمانند مشبک ایجاد میکنند و فضای بین سلولها را پر میکنند و مانعی برای مولکولهای بزرگ و میکروارگانیسمها هستند.
نماینده دیگر پروتئوگلیکان ها هپارین است که شامل چندین زنجیره سولفاته هتروپلی ساکارید مرتبط با هسته پروتئین از طریق باقی مانده های سرین است. در خون، هپارین به آنتی ترومبین III متصل می شود و مجموعه ای را تشکیل می دهد که فاکتورهای انعقاد خون IIa، IXa، Xa، XIa و XIIa را مسدود می کند، که برای جلوگیری از ترومبوز در بیماران با پروفایل های مختلف استفاده می شود. در حال حاضر از فرآورده های هپارین های با وزن مولکولی کم و هپارین های شکسته نشده با ویژگی های بهتر استفاده می شود.
همچنین، عملکرد هپارین یک اثر فعال کننده بر فعالیت آنزیم لیپوپروتئین لیپاز است که در متابولیسم اشکال انتقال لیپیدها در خون (شیلومیکرون ها و لیپوپروتئین های با چگالی بسیار کم) نقش دارد. در نتیجه میزان لیپیدهای خون کاهش می یابد.
روش های مطالعه محتوای پروتئین های حاوی کربوهیدرات
هنگام مطالعه محتوای پروتئین های حاوی کربوهیدرات، می توان از چندین روش روش شناختی استفاده کرد:
تفاوت رنگ پس از واکنش های کربازول و اورسین، قضاوت در مورد محتوای نسبی سولفات درماتان را در نمونه ممکن می سازد. برای نمونه خالص سولفات درماتان، نسبت محتوای گلیکوزآمینوگلیکان ها با توجه به واکنش کاربازول به غلظت آنها، که توسط واکنش ارسین تعیین می شود، 0.67 است. در حضور سایر گلیکوزامینوگلیکان ها (به جز کراتان سولفات)، ضریب افزایش می یابد.
روش رزورسینول برای تعیین غلظت اسیدهای سیالیک و روش اورسین برای تعیین تمام هگزوزهایی که گلیکوپروتئین ها و هگزوزهای مرتبط با سروگلیکوئیدها را تشکیل می دهند به عنوان یکپارچه تایید شده اند.
روش رزورسینول برای تعیین غلظت اسیدهای سیالیک (طبق نظر Svennerholm)
اصل
هنگامی که گلیکوپروتئین های پلاسما با اسید تری کلرواستیک گرم می شوند، اسیدهای سیالیک جدا می شوند که به نوبه خود هیدرولیز می شوند و اسید نورآمینیک را تشکیل می دهند. رزورسینول در حضور نمک های مس در محیط اسید هیدروکلریک رنگ آبی با اسید نورآمینیک می دهد.
مقادیر نرمال
غلظت اسیدهای سیالیک در خون با فرآیندهای التهابی مختلف (اندوکاردیت، استئومیلیت)، با سل، لوسمی، لنفوگرانولوماتوز، نفروز افزایش می یابد، به شدت با تومور مغزی، انفارکتوس میوکارد افزایش می یابد، با آسیب به پارانشیم کبد، کلاژنوزها و غیره افزایش می یابد. فرآیندهایی که با تخریب بافت همبند رخ می دهد.
کاهش سطح سرمی اسیدهای سیالیک در بیماران مبتلا به کم خونی پرنیشیوز، هموکروماتوز، بیماری ویلسون و فرآیندهای دژنراتیو در سیستم عصبی مرکزی مشاهده می شود.
تعیین محتوای سروموکوئیدها و مقدار کل گلیکوپروتئین ها به روش اورسی
اصل
گلیکوپروتئین ها همراه با پروتئین های سرم یا پلاسما با الکل رسوب می کنند، رسوب شسته می شود، در قلیایی حل می شود و پس از هیدرولیز با اسید سولفوریک، غلظت هگزوزها با واکنش با اورسین تعیین می شود که با محتوای گلیکوپروتئین ها مطابقت دارد.
برای تعیین سروموکوئیدها، پروتئین ها با اسید پرکلریک رسوب می کنند، در حالی که سروموکوئیدها رسوب نمی کنند. سپس با استفاده از اسید فسفو تنگستیک، سروموکوئیدها از مایع رویی رسوب داده شده، رسوب شسته شده و پس از حل شدن در قلیایی، سطح هگزوزها تعیین می شود.
مقادیر نرمال
ارزش بالینی و تشخیصی
میزان گلیکوپروتئین های هگزوز در فرآیندهای التهابی مختلف افزایش می یابد: سل، پلوریت، پنومونی، روماتیسم حاد، گلومرولونفریت، دیابت، انفارکتوس میوکارد، نقرس، نئوپلاسم های بدخیم. تعیین غلظت گلیکوپروتئین ها در بیماری های تنبل از اهمیت ویژه ای برخوردار است، در حالی که افزایش فعالیت نشان دهنده فعال شدن فرآیند است، اگرچه علائم بالینی ممکن است هنوز ظاهر نشود.
گلیکوزامینوگلیکان ها داروهایی هستند که قبلا موکوپلی ساکاریدها نامیده می شدند. در بدن، این مواد به صورت کووالانسی به پروتئوگلیکان ها متصل می شوند و به صورت آزاد وجود ندارند. در مجموع، امروزه مرسوم است که 7 نوع اصلی را تشخیص دهیم که 6 نوع از آنها از نظر ساختار مشابه هستند. این:
- سولفات درماتان.
- کندرویتین-4-سولفات.
- کندورویتین-6-سولفات.
- هپارین.
- هپاران سولفات.
در مورد نوع هفتم، این کراتان سولفات است که کمی با موارد فوق متفاوت است. در بدن، همه این مواد بخشی از بافت همبند ماده بین سلولی هستند، در بافت استخوان و مایع سینوویال و همچنین در بدن زجاجیه و قرنیه چشم یافت می شوند. آسیب شناسی ژنتیکی تجزیه گلیکوزامینوگلیکان ها به ایجاد چنین بیماری ارثی مانند موکوپلی ساکاریدوز ختم می شود.
آرترادول
یک آمپول از این دارو حاوی 100 میلی گرم کندرویتین سولفات سدیم است. در صورت تزریق عضلانی، به راحتی جذب می شود و پس از 15 دقیقه در مایع سینوویال یافت می شود. بیشترین غلظت یک ساعت پس از مصرف مشاهده می شود، سپس به تدریج طی دو روز کاهش می یابد.
در طول دوره درمان، دارو با 100 میلی گرم یک روز در میان استفاده می شود. ماده خشک ابتدا باید در 1 میلی لیتر آب تزریقی رقیق شود. دوره کامل درمان 25-35 تزریق است، پس از 6 ماه دوره می تواند تکرار شود.
نشانه های اصلی مصرف دارو آرتروز اولیه، آرتروز با آسیب به بزرگترین مفاصل و استئوکندروز بین مهره ای است.
آرترون کندرکس
این یک قرص مدرن بر پایه کندرویتین سولفات است و هر قرص حاوی 750 میلی گرم ماده فعال است. در درمان بیماری های مختلف استفاده می شود:
- استئوپاتی
- پریودنتوپاتی ها
- استئوکندروز.
- بیماری های دژنراتیو غضروف و مفاصل.
یک تا دو قرص باید در روز مصرف شود. پس از دستیابی به اثر مطلوب، دوز به دوز نگهدارنده 750 میلی گرم در روز کاهش می یابد.
آنژیوفلاکس
ماده فعال این دارو یک محصول طبیعی است که از مخلوطی از گلیکوزامینوگلیکان ها - یک کسر هپارین مانند و سولفات درماتان تشکیل شده است. این دارو به صورت قطره ای به صورت داخل وریدی تجویز می شود و محتویات آمپول را در 150-200 میلی لیتر سالین حل می کند. دوره تجویز تزریقی 15-20 سیستم است، پس از آن باید به مصرف کپسول بروید.
نشانه های اصلی برای پذیرش آنژیوپاتی است که در آن خطر ترومبوز، میکروآنژیوپاتی، که شامل نفروپاتی، رتینوپاتی، نوروپاتی و ماکروآنژیوپاتی در دیابت است، وجود دارد.
وسل دو اف
این دارو به صورت کپسول و محلول برای تجویز عضلانی و داخل وریدی تولید می شود و به داروهای ضد انعقاد مستقیم اثر اشاره دارد. در ابتدای درمان، دارو به صورت داخل وریدی تجویز می شود و پس از آن به مصرف کپسول تغییر می کند. مدت درمان 30 تا 40 روز است. دوره کامل دو بار در سال برگزار می شود. نشانه های اصلی برای استفاده عبارتند از:
- آنژیوپاتی با افزایش خطر ترومبوز.
- سکته مغزی ایسکمیک.
- زوال عقل عروقی
- فلبوپاتی.
- شرایط ترومبوفلبی
- ترومبوسیتوپنی ترومبوتیک ناشی از هپارین.
در طول دوره درمان، نظارت مداوم بر خون محیطی و همچنین زمان خونریزی و زمان لخته شدن لازم است.
موکارترین
 موکارترین دارویی است که به محرک های بازسازی بافت غضروف تعلق دارد. این دارو دارای فعالیت ضد التهابی خوبی است، دارای اثر ضد ترومبوتیک است، سطح لیپیدها را در خون کاهش می دهد، به بازسازی بافت همبند آسیب دیده و سلول های غضروف کمک می کند.
موکارترین دارویی است که به محرک های بازسازی بافت غضروف تعلق دارد. این دارو دارای فعالیت ضد التهابی خوبی است، دارای اثر ضد ترومبوتیک است، سطح لیپیدها را در خون کاهش می دهد، به بازسازی بافت همبند آسیب دیده و سلول های غضروف کمک می کند.
قبل از شروع درمان با هر دارویی از گروه گلیکوزامینوگلیکان ها، باید با یک متخصص مشورت کنید، زیرا ممکن است موارد منع مصرف وجود داشته باشد و برای هر 7 نوع از این مواد می توانند بسیار متفاوت باشند، زیرا داروها متفاوت عمل می کنند.
داروهایی که نیز به این گروه تعلق دارند عبارتند از:
- ساختار.
- کندروگارد.
- کندرویتین.
- کندروکسید.
- رومالون.
چه چیزی می تواند با کمبود گلیکوزامینوگلیکان ها مرتبط باشد؟ این ممکن است نتیجه رژیم غذایی یا گیاهخواری، اختلالات متابولیک که منجر به بیماری می شود، استرس بیش از حد بر بدن و تغییرات مرتبط با افزایش سن باشد. بنابراین، در برخی موارد، داروهای حاوی گلیکوزامینوگلیکان ها ممکن است برای پیشگیری تجویز شود.
فرمول های ساختاری در طرح ریزی فیشر قادر به ارائه یک تصویر هندسی جامع از ساختار همی استال نیستند، زیرا آنها زوایای فضایی واقعی بین پیوندهای شیمیایی را منعکس نمی کنند. در سال 1929 هاورثروشی را برای به تصویر کشیدن اشکال حلقوی کربوهیدراتها پیشنهاد کرد که ساختارهای واقعی را بیشتر منعکس میکند. ساختارهای حلقوی پنج و شش عضوی به شکل سیستمهای حلقوی مسطح به تصویر کشیده میشوند که گروههای هیدروکسیل در هر اتم کربن آنها به سمت بالا یا پایین جهتگیری شدهاند. معمولاً از شکل ساده شده ای برای نوشتن فرمول در طرح Haworth استفاده می شود که اتم های کربن موجود در حلقه را حذف می کند. برای تبدیل فرمول ها Dمونوزها در طرح فیشر در فرمول هاورث، قوانین خاصی باید رعایت شود: 1. همه گروه هایی که در سمت راست هسته کربن در فرمول های فیشر قرار دارند، در فرمول های هاورث، موقعیتی را در زیر صفحه حلقه اشغال می کنند (در زیر). ). 2. گروه هایی که در فرمول های فیشر در سمت چپ هسته کربن قرار دارند در بالای صفحه حلقه (بالا) قرار دارند. 3. گروه انتهایی - CH 2 OH در برجستگی هاورث به سمت بالا هدایت می شود. در محلول، اشکال خطی و حلقوی مونوساکاریدها به طور همزمان وجود دارند و می توانند خود به خود به یکدیگر تبدیل شوند. این اشکال ایزومری نامیده می شوند توتومرهای زنجیره حلقه. به عنوان یک قاعده، ایزومرهای حلقوی پلی ساکاریدها غالب هستند. آنها توسط ارگانیسم ها برای ساختن الیگو و پلی ساکاریدها، مونونوکلئوتیدها و سایر مولکول های بیولوژیکی استفاده می شوند. یک انتقال از طریق فرم خطی وجود دارد α -در β -شکل. گروه هیدروکسیل که از بسته شدن حلقه از کربونیل تشکیل می شود نامیده می شود همی استالیا هیدروکسیل گلیکوزیدی. مشتقات مونوساکارید: گروه بزرگی از مشتقات مونوساکارید، استرهای فسفریک هستند که در طی تبدیل کربوهیدرات ها در بافت ها به وجود می آیند: گلیسرآلدئید-3-فسفات. β-D-ریبوز-5-فسفات α-D-ریبوز-1-فسفات β-D-فروکتوز-1،6-دی فسفات دو مشتق آمینو از مونوساکاریدها به طور گسترده در طبیعت توزیع شده اند: گلوکزامین و گالاکتوزامین. مانند هگزوزهای مربوطه، هگزوزامین ها می توانند به دو شکل خطی و حلقوی وجود داشته باشند. گلوکزآمین جزء بسیاری از پلی ساکاریدهای موجود در بافت های حیوانی و انسانی است. گالاکتوزامین جزء گلیکوپروتئین ها و گلیکولیپیدها است. گلوکوزامین گالاکتوزامین گلوکورونیک اسید پلی ساکاریدها حاوی اسید گلوکورونیک هستند. عملکردهای بیولوژیکی مونوساکاریدها:- انرژی - مونوساکاریدها به عنوان منابع انرژی در سلول استفاده می شوند.
- پلاستیک - مونوساکاریدها و مشتقات آنها در ساخت مولکول های بیولوژیکی مختلف نقش دارند.
- ساختار مونوساکاریدهایی که زنجیره را تشکیل می دهند.
- نوع پیوندهای گلیکوزیدی که مونومرها را در زنجیره به هم متصل می کند.
- توالی باقی مانده های مونوساکارید در زنجیره
- پلی ساکاریدهای ساختاری که استحکام مکانیکی سلول ها و اندام ها را تامین می کنند.
- پلی ساکاریدها که بخشی از ماتریکس خارج سلولی هستند در تشکیل بافت ها و همچنین در تکثیر و تمایز سلول ها شرکت می کنند. پلی ساکاریدهای ماتریکس بین سلولی محلول در آب و بسیار هیدراته هستند.