التكوين هو الترتيب المكاني النسبي للذرات أو المجموعات الذرية في الجزيء الكبير ، والذي يتم ضبطه أثناء عملية التخليق ولا يمكن تغييره دون كسر الروابط الكيميائية للسلسلة الرئيسية.
هناك ثلاثة أنواع من التماكب التكويني: التماكب المحلي ، رابطة الدول المستقلة عبرايزومرية و فرايزوميريزم.
التماثل الموضعي هو سمة مميزة للبوليمرات ذات وحدة التكرار غير المتماثلة (بوليمرات فينيل وفينيدين ، (ميثاكريلات ، إلخ). لذلك ، بالنسبة لجزيء فينيل مونومر
البدائل في ذرات C (1) (رأس) و (2) (ذيل) تختلف ، وبالتالي ، هناك ثلاثة أنواع من الإضافة ممكنة (في دياد ، أي في وحدتين مونومر متتاليتين):

التعلق من الرأس إلى الرأس أقل احتمالية من التعلق من الرأس إلى الذيل ، ويرجع ذلك أساسًا إلى العائق الستيري. لذلك ، على سبيل المثال ، في فلوريد البولي فينيلدين (-CH 2 -CF 2 -) "وبولي ميثيل ميثاكريلات ، لا تتجاوز نسبة الوحدات المرفقة وفقًا لنوع" الرأس - الرأس "5-6٪.
من الممكن أيضًا إرفاق المونومرات وفقًا لنوع "الذيل - الذيل" ، ومع ذلك ، لا يمكن تمييز هذا النوع من التماثل إلا لثنائيات من الوحدات المتكررة ، وفي الجزيء الكبير الفرق بين "الذيل - الذيل" و "الرأس - مرفقات الرأس "مستوية.
ايزومرية رابطة الدول المستقلةسمة من سمات البوليمرات التي تحتوي على روابط مزدوجة في السلسلة الرئيسية (polydienes ، polyacetylenes) ، وتتكون من إمكانية ترتيب البدائل واحدًا تلو الآخر (ايزومر رابطة الدول المستقلة)أو على طرفي نقيض (نشوة-ايزومر) لمستوى الرابطة المزدوجة:

الأيزومرية الفراغيةوضوحا للبوليمرات الاصطناعية التي تحتوي على ذرات كربون غير متماثلة في السلسلة الرئيسية ، وكذلك لمجموعة واسعة من البوليمرات الطبيعية مثل البروتينات والسكريات والأحماض النووية.
في هذه الحالة ، هناك خياران ممكنان:
- 1) تحتوي الجزيئات الكبيرة في السلسلة الرئيسية ذرة كربون غير متماثلة حقيقيةويعرض نشاطًا بصريًا (أكسيد بولي بروبيلين ، بوليمرات طبيعية) ؛
- 2) الجزيئات مع ذرة كربون غير متماثلة زائفةالتي لا تظهر نشاطا بصريا.
في البوليمرات الحيوية ، يتم تضمين ذرات الكربون غير المتماثلة (المميزة؟) في جزيئات المركبات الأحادية الأولية - الأحماض الأمينية والكربوهيدرات (الريبوز والجلوكوز وما إلى ذلك):

وتبقى في كل رابط من الجزيئات الكبيرة بعد تركيبها ، على سبيل المثال ، في polypeptides (poly - / _- alanine) و polysaccharides (amylose): 
بولي 1،4-أ ، د-غلوكوبيرانوسيد (أميلوز)
نتيجة لذلك ، تتمتع البوليمرات الحيوية بنشاط بصري عالٍ. في فئة البوليمرات الاصطناعية ، تعتبر الأيزومرية الفراغية سمة أساسية لسلسلة الكربون الفينيلو فينيلدينالبوليمرات ، التي يظهر هيكلها بشكل تخطيطي أدناه.

في هذه الحالة ، يرجع التماثل المرصود إلى الاختلاف في تكوين ذرة الكربون رباعي السطوح التي تحتوي على بديل غير هيدروجين X أو بدائل X و Z.
بالمعنى الدقيق للكلمة ، فإن ذرات الكربون هذه غير متماثلة لأنها مرتبطة بأربع مجموعات مختلفة (X ، H أو X ، Z) واثنين من قطع السلسلة التي تختلف في الطول ومجموعات النهاية. ومع ذلك ، فإن هذه البوليمرات لا تظهر خصائص بصرية بسبب عدم تناسق أقرب بيئة لذرات الكربون ، حيث أن مجموعات CH 2-CHX أو CH 2 -CXZ تجاور ذرة الكربون غير المتماثلة على كلا الجانبين ، وبالتالي تسمى هذه الذرات زائف غير متماثل.يصف المفهوم انتظام وطبيعة ترتيب مراكز الأيزومرية الفراغية هذه "براعة".دعونا نفكر في هذا النوع من الأيزومرية بمزيد من التفصيل باستخدام بوليمر الفينيل كمثال.


نظرًا لتقويمها إلى أقصى حد دون انتهاك زوايا الرابطة ، تتخذ السلسلة الهيكلية لمثل هذا البوليمر ذي السلسلة الكربونية شكل متعرج مسطح ويمكن وضعها في مستوى النمط. في هذه الحالة ، يتم توجيه البدائل الموجودة في ذرة الكربون ، والتي يشار إلى روابطها بخطوط سميكة ، نحو القارئ ، ويتم توجيه البدائل ، التي يشار إلى روابطها بخطوط رفيعة ، بعيدًا عن القارئ.
دعونا نطبق الطريقة المبسطة التي اقترحها عام 1891 الكيميائي العضوي الألماني E. Fischer لتحديد وعرض الأيزومرات الفراغية. لنقم بإسقاط سلسلة البوليمر الموضحة أعلاه على مستوى عمودي على مستوى الصفيحة. نتيجة لذلك ، نحصل على إسقاط فيشر ، حيث توجد جميع البدائل X بخلاف الهيدروجين على جانب واحد من المستوى عموديًا على الصفيحة. يسمى هذا الأيزومير الفراغي متماثل.

هناك متغير آخر لترتيب البدائل X واضح أيضًا ، وهو التناوب الصارم للبدائل X على جوانب مختلفة من المستوى. يسمى هذا الأيزومير الفراغي متلازم.

بعبارات أخرى، بوليمر متماثلعبارة عن بوليمر ، كل وحدة مونومر تحتوي على مركز واحد من الأيزوميرات الفراغية وتكوين هذه المراكز هو نفسه ، و البوليمر المتلازمي -إنه بوليمر ، كل وحدة مونومر تحتوي على مركز واحد من الأيزوميرات الفراغية والوحدات المجاورة لها تكوينات معاكسة. إذا كان موقع البديل X عشوائيًا ، فلا يوجد تنظيم مجسم ، ويشار إلى مثل هذا الأيزومر التكويني على أنه رقيق.
تشير البيانات المعطاة إلى البوليمرات التي توجد لها ذرة كربون واحدة غير متماثلة في وحدة التكرار. لاحظ أن تسمى هذه الجزيئات الكبيرة أحادي.في وعظيفي البوليمرات ، تحتوي وحدة التكرار على ذرتين غير متماثلتين زائفتين.
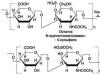
ثنائي الخواصيتم الحصول على البوليمرات على أساس ألكينات 1،2-disubstituted للهيكل العام (CHR = CHR "). في هذه الحالة ، لا يعتمد هيكل منتج البوليمر على التناوب فقط L-و D-isomers في جزيء المونومر ، ولكن أيضًا في تماثله الهندسي. على سبيل المثال ، بالنسبة لـ 14 مجم: - أيزومر ، يتكون بوليمر ثنائي التباين:

مطهرتشكل البوليمرات أيضًا بنيتين متلازمتين ( إرثرو- و تريو) ،التي يتطابق فيها هيكل السلسلة الرئيسية.

من المعروف أن البوليمرات الاصطناعية تحتوي على ذرات كربون غير متناظرة ، ونتيجة لذلك ، يكون لها نشاط بصري. الممثل النموذجي لهذه المركبات هو أكسيد البولي بروبلين، يتم عرض إسقاط فيشر أدناه (يشار إلى ذرات الكربون غير المتماثلة بواسطة *).

أمثلة أخرى للبوليمرات النشطة بصريًا هي مادة البولي أميد التي تعتمد على (+) - 2،2 "-ديامينوبينافثيل -1 ، و G و terephthaloyl chloride

وأيضًا مادة البولي أميد التي يتم الحصول عليها عن طريق التكثيف المتعدد لـ f-lysine وثاني كلوريد حمض الأديبيك في وجود أيونات النحاس: 
يتم الحصول على البوليمرات الاصطناعية النشطة بصريًا:
- 1) البوليمر غير النشط ، مما يؤدي إلى إدخال مجموعات نشطة بصريًا في بدائلها الجانبية أو إلى إنشاء مراكز غير متماثلة عن طريق التوليف غير المتماثل ؛
- 2) البلمرةأو متعدد التكثيفالمونومرات النشطة بصريًا ، والتي تحدث في ظل ظروف تمنع العنصرية ؛
- 3) التحولات البوليمرية المماثلةبوليمرات نشطة بصريا
- 4)البلمرة الانتقائية الفراغيةأحد الأيزومرين البصريين الموجودين في الخليط الراسيمي للمونومر ؛
- 5) التوليف غير المتماثل -البلمرة الفراغية النوعية أو الإضافة المتعددة للمونومرات المتماثلة.
تكوين التكوين المعقد نموذجي لـ بوليمرات ديين.أثناء بلمرة البوتادين المتماثل ، تكون الإضافة ممكنة بسبب فتح روابط 1،2- أو الفتح المتزامن لـ 1،2- و 3،4- روابط (1،4-إضافة). والنتيجة هي خليط من منتجي بوليمر مختلفين: 1،4-بولي بوتادين و 1،2-بولي بوتادين:

بالنسبة للأول ، m ، من الممكن أن يكون تكوين is-trans isomerism ، وللحالة الثانية ، isomerism المحلية و stereoisomerism.
يصبح الوضع أكثر تعقيدًا أثناء بلمرة الديانات غير المتكافئة (على سبيل المثال ، الأيزوبرين) ، والتي لوحظ فيها إضافة 1،4- و 1،2- و 3،4:

في أي نوع من البلمرة ، يحدث تكوين أيزومرات محلية. على غرار الحالة المذكورة أعلاه ، يتميز 1.4-بولي إيزوبرين بالإضافة إلى ذلك بـ r ^ r / c-oprais-isomerism و 1،2- و 3،4-polyisoprene - بواسطة الأيزومرية الفراغية.
يعد تكوين تكوين معين في عملية تخليق البوليمر ، وكذلك دراسة التركيب التكويني للجزيئات الكبيرة ، أحد أهم المشكلات في الكيمياء التركيبية والفيزيائية للبوليمرات. ترتبط بنية البوليمرات ككل وخصائصها الفيزيائية والميكانيكية ارتباطًا وثيقًا بالتكوين. تتبلور البوليمرات المجسمة ، كقاعدة عامة ، بسهولة ، بينما يمكن أن توجد البوليمرات غير المتبلورة إلا في حالة الطور غير المتبلور. على سبيل المثال ، كلوريد البوليفينيل المتساوي هو بوليمر بلوري مع نقطة انصهار 240 درجة مئوية ، والبولي فينيل كلوريد غير متبلور مع درجة حرارة انتقال الزجاج 90 درجة مئوية. درجة حرارة التزجج لبولي ميثيل ميثاكريلات متساوي التوضيع هي 40 درجة مئوية ، ودرجة حرارة التزجج هي 160 درجة مئوية. المطاط الطبيعي (1.4-gshs-polyisoprene) هو مادة ناعمة ومرنة بدرجة حرارة انتقال زجاجي تقل عن 73 درجة مئوية ، gutta-percha
(1،4-7iryans-polyisoprene) عبارة عن بوليمر بلوري بنقطة انصهار تبلغ 43 درجة مئوية.
تتمتع البوليمرات النشطة بصريًا بخصائص ميكانيكية أعلى ومقاومة أعلى للحرارة من المنتجات الراسيمية ؛ وهي مناسبة لتصنيع الزجاج والأفلام القادرة على تدوير مستوي استقطاب الضوء المرسل (الأجهزة البصرية ومرشحات الضوء). إن أهم مجال لتطبيق البوليمرات النشطة بصريًا هو فصل الأيزومرات الضوئية بالطرق الكروماتوجرافية واستخدامها كمحفزات في التخليق العضوي غير المتماثل وكمصفوفة في التخليق غير المتماثل للبوليمرات.
يتم تحديد التكوينات المحلية من الرأس إلى الذيل ومن الرأس إلى الرأس باستخدام طريقة الرنين المغناطيسي النووي (NMR). تعتمد خصائص إشارة الذرات البديلة الجانبية التي تم تحديدها بواسطة هذه الطريقة (1H ، 13C ، 15N ، 19F) المرتبطة بتفاعل دوران هذه النوى على المسافة المتبادلة بينهما على طول سلسلة البوليمر ، مما يجعل من الممكن تقدير النسبة من الإضافات من الرأس إلى الذيل. يكمن نفس المبدأ في تعريف الأيزومرية الفراغية للجزيئات الكبيرة: في التكوين متساوي التوضيع ، تكون المجموعات الجانبية على مسافة أصغر من بعضها البعض مقارنة بالمجموعة المتزامنة. باستخدام طريقة الرنين المغناطيسي النووي عالية الدقة ، والتي تحدد المجموعات الجانبية ، من الممكن إصلاح الإشارات من الوحدات الأحادية المكونة لعدسات متساوية ، وسانديو ، وغيرية ، ولحساب نسبة هذه الثلاثيات وتوزيعها في سلاسل البوليمر.
العواقب البيولوجية لأكسدة الدهون
زيادة تكوين الجذور الحرة في الجسم والزيادة المصاحبة في عمليات بيروكسيد الدهون (تسمى أحيانًا "الإجهاد التأكسدي") مصحوبة بعدد من الاضطرابات في خصائص الأغشية البيولوجية وعمل الخلية. تتلف هياكل البروتين أو طبقة الدهون الثنائية ككل. عواقب بيروكسيد الدهون. التأثير الضار لأكسدة سلسلة الدهون على الأغشية البيولوجية ناتج عن أكسدة مجموعات ثيول من البروتينات ، وزيادة في نفاذية الأغشية الأيونية ، وانخفاض القوة الكهربائية للطبقة الدهنية للأغشية ، مما يؤدي إلى "ذاتية- انهيار "الأغشية بواسطة مجال كهربائي. طورت الخلية الحية نظامًا كاملاً للحماية من الضرر الذي تسببه الجذور الحرة. أولاً ، يترافق بيروكسيد الدهون مع أكسدة مجموعات ثيول (سلفهيدريل) من بروتينات الغشاء (Pr).
Pr-SH + R -> RH + Pr-S
Pr-S + O 2 -> Pr-SO 2 -> المشتقات الجزيئية
تنتهي أكسدة البروتينات المرتبطة ببيروكسيد الدهون وتكوين تجمعات البروتين في عدسة العين بغشاؤها ؛ تلعب هذه العملية دورًا مهمًا في تطور الشيخوخة وأنواع أخرى من إعتام عدسة العين لدى البشر. يلعب أيضًا تعطيل إنزيمات النقل الأيوني دورًا مهمًا في علم أمراض الخلايا ، حيث يشتمل مركزها النشط على مجموعات ثيول ، في المقام الأول Ca2 + -ATPase ، مما يؤدي إلى زيادة تركيز أيونات الكالسيوم داخل الخلايا وتلف الخلية. ترتبط النتيجة الثانية لبيروكسيد الدهون بحقيقة أن منتجات البيروكسيد لديها القدرة على زيادة نفاذية الأيونات للطبقة الدهنية الثنائية بشكل مباشر. وهكذا ، تبين أن منتجات بيروكسيد الدهون تجعل الطور الدهني للأغشية منفذاً لأيونات الهيدروجين والكالسيوم. يؤدي هذا إلى حقيقة أن الأكسدة والفسفرة في الميتوكوندريا غير منفصلين ، وتجد الخلية نفسها في ظروف مجاعة للطاقة (أي نقص ATP). في الوقت نفسه ، تدخل أيونات الكالسيوم إلى السيتوبلازم ، مما يؤدي إلى تلف الهياكل الخلوية. النتيجة الثالثة (وربما الأكثر أهمية) للأكسدة هي انخفاض في استقرار طبقة الدهون ، مما قد يؤدي إلى انهيار كهربائي للغشاء من خلال إمكانات الغشاء الخاصة به ، أي تحت تأثير الاختلاف في الجهود الكهربائية الموجودة على أغشية الخلية الحية. يؤدي الانهيار الكهربائي إلى فقدان الغشاء الكامل لوظائف الحاجز.
يتم تحديد التنوع الهائل لوظائف الجزيئات الكبيرة في الخلية من خلال تنظيمها المكاني. لذلك ، فإن إحدى أهم مهام الفيزياء الحيوية الجزيئية هي توضيح الأسس الفيزيائية لتشكيل التركيب المكاني والخصوصية البيولوجية. يشير هذا إلى حقيقة أن النشاط البيولوجي حساس للتغيرات في التركيب المكاني للجزيئات الكبيرة.
حاليًا ، يتم تمييز عدة مستويات بشكل تقليدي بحت - الابتدائية والثانوية والثالثة والرباعية.
الهيكل الأساسي للجزيئات الكبيرة- سلسلة من الروابط في سلسلة البوليمر الحيوي مرتبطة ببعضها البعض بواسطة روابط تساهمية قوية. في البروتينات ، هذا هو تسلسل الأحماض الأمينية ، وفي NK هو تسلسل النيوكليوتيدات. تتشكل سلاسل البوليمرات بواسطة روابط تساهمية قوية.
الهيكل الثانويهو محلي ، أي الترتيب المحلي للأقسام الفردية للجزيئات الحيوية (الهيكل المرتب للسلسلة الرئيسية للبوليمر الحيوي).
تحت الهيكل الثالثفهم التخطيط المكاني للكل. هيكل رباعي- يُفهم على أنه الترتيب المكاني للعديد من سلاسل البوليمر المنظمة بشكل مضغوط ، سلاسل مع تكوين مجمع فوق الجزيئي.
إذن ما هو المقصود بالتشكيل؟ تشكيل جزيء ضخم- هذه طريقة لوضع سلسلة بوليمر (بدون كسر الروابط التساهمية) بسبب تكوين عدد كبير من الروابط الضعيفة ، ونتيجة لذلك يتم تشكيل الهيكل المكاني الأكثر ملاءمة وثباتًا للديناميكية الحرارية للجزيء الكبير. تؤدي التغييرات في المعلمات البيئية (درجة الحرارة ، ودرجة الحموضة ، والقوة الأيونية ، وعمل عوامل تغيير الطبيعة) إلى إعادة ترتيب مطابقة للجزيئات الحيوية مع تكوين بنية مكانية مستقرة جديدة.
يمكن تقسيم جميع أنواع التفاعلات بين الذرات ، بغض النظر عن طبيعتها الفيزيائية ، أثناء تكوين روابط جزيئية مختلفة إلى نوعين رئيسيين:
1. التفاعلات قصيرة المدى بين ذرات الوحدات المجاورة (الروابط التساهمية).
2. التفاعلات طويلة المدى بين الذرات ، والتي على الرغم من أنها متباعدة على طول السلسلة ، إلا أنها تلتقي عرضيًا في الفضاء نتيجة لانحناءات السلسلة (تفاعلات ضعيفة - قوى فان دير فالس ، قوى كارهة للماء ، التفاعلات الكهروستاتيكية والروابط الهيدروجينية).
مقدمة
جزيئات البوليمر هي فئة واسعة من المركبات ، الأساسيةالخصائص المميزة لها هي الوزن الجزيئي الكبير والمرونة التوافقية العالية للسلسلة. يمكن القول بثقة أن جميع الخصائص المميزة لهذه الجزيئات ، بالإضافة إلى إمكانيات تطبيقها المرتبطة بهذه الخصائص ، ترجع إلى الميزات المذكورة أعلاه.
لذلك ، من الأهمية بمكان دراسة إمكانية التنبؤ المسبق بالسلوك الكيميائي والفيزيائي للبوليمر بناءً على تحليل هيكله. يتم توفير هذه الفرصة من خلال طرق الميكانيكا الجزيئية والديناميات الجزيئية ، التي يتم تنفيذها في شكل برامج حساب الكمبيوتر.
باستخدام هذه الطرق ، تم إجراء الحساب النظري للتشكيل الأكثر احتمالا لبعض الأوليغومرات مع عدد الوحدات المونومرية من 50 إلى 100. تم الحصول على البيانات التي جعلت من الممكن تحديد التشكل الأكثر احتمالا للجزيئات ، حجم Kuhn ، وعدد المخلفات الأحادية في المقطع.
مراجعة الأدبيات
I. البوليمرات. ملامح الهيكل والخصائص.
البوليمرات هي مواد جزيئية عالية ، تتكون جزيئاتها من عناصر هيكلية متكررة - روابط متصلة في سلاسل بواسطة روابط كيميائية ، بكمية كافية لحدوث خصائص محددة. يجب أن تُعزى القدرات التالية إلى خصائص معينة:
1. القدرة على تشوهات عالية المرونة قابلة للانعكاس الميكانيكي ؛
2. لتشكيل الهياكل متباينة الخواص.
3. لتكوين محاليل عالية اللزوجة عند التفاعل مع مذيب ؛
4. إلى تغيير حاد في الخصائص عند إضافة إضافات ضئيلة من مواد ذات وزن جزيئي منخفض.
يمكن شرح الميزات الفيزيائية والكيميائية المعطاة على أساس فهم بنية البوليمرات. عند الحديث عن التركيب ، ينبغي للمرء أن يشير ضمنيًا إلى التركيب الأولي للمادة ، وترتيب روابط الذرات ، وطبيعة الروابط ، ووجود تفاعلات بين الجزيئات. من خصائص البوليمرات وجود جزيئات طويلة السلسلة مع اختلاف حاد في طبيعة الروابط على طول السلسلة وبين السلاسل. وتجدر الإشارة بشكل خاص إلى عدم وجود جزيئات سلسلة معزولة. يتفاعل جزيء البوليمر دائمًا مع البيئة ، والتي يمكن أن يكون لها طابع بوليمر (حالة البوليمر النقي) وخاصية السائل العادي (محاليل البوليمر المخففة). لذلك ، لتوصيف البوليمر ، لا يكفي تحديد نوع الروابط على طول السلسلة - من الضروري أيضًا الحصول على معلومات حول طبيعة التفاعل بين الجزيئات. يجب أن يؤخذ في الاعتبار أنه لا يمكن إدراك الخصائص المميزة للبوليمرات إلا عندما تكون الروابط الموجودة على طول السلسلة أقوى بكثير من الروابط المتقاطعة التي تشكلت بسبب التفاعلات بين الجزيئات من أي أصل. هذه هي بالضبط السمة الرئيسية لهيكل أجسام البوليمر. لذلك ، يمكن القول أن المجمع الكامل للخصائص الشاذة للبوليمرات يتم تحديده من خلال وجود جزيئات سلسلة خطية مع تفاعل جزيئي ضعيف نسبيًا. يؤدي تفرع هذه الجزيئات أو ارتباطها بشبكة إلى إدخال بعض التغييرات في مجمع الخصائص ، ولكنه لا يغير حالة الأمور من حيث الجوهر طالما بقيت المقاطع الخطية طويلة السلسلة بشكل كافٍ. على العكس من ذلك ، يؤدي فقدان البنية المتسلسلة للجزيئات أثناء تكوين الكريات أو الشبكات الكثيفة منها إلى فقدان كامل مجموعة الخصائص المميزة للبوليمرات.
نتيجة ما سبق هو ظهور مرونة جزيء السلسلة. يكمن في قدرته على تغيير الشكل تحت تأثير الحركة الحرارية للوصلات أو المجال الخارجي الذي يوضع فيه البوليمر. ترتبط هذه الخاصية بالدوران الداخلي للأجزاء الفردية للجزيء بالنسبة لبعضها البعض. في جزيئات البوليمر الحقيقية ، يكون لزوايا الرابطة قيمة محددة جيدًا ، ولا توجد الروابط بشكل عشوائي ، ويتضح أن موضع كل رابط لاحق يعتمد على موضع الارتباط السابق.
تسمى البوليمرات التي تظهر اهتزازات التوائية شديدة بدرجة كافية سلسلة مرنة ،والبوليمرات التي يصعب فيها دوران جزء من السلسلة بالنسبة إلى الجزء الآخر - سلسلة جامدة.
هذا يعني أنه يمكن للجزيئات أن تدور وتغير بنيتها دون كسر الروابط الكيميائية ، وتشكيل تشكيلات مختلفة ، والتي تُفهم على أنها أشكال مكانية مختلفة للجزيء الذي ينشأ عندما يتغير الاتجاه النسبي لأجزائه الفردية نتيجة للدوران الداخلي للذرات أو المجموعات. من الذرات حول روابط بسيطة ، وثني السندات ، وما إلى ذلك.
ثانيًا. التحليل التوافقي للبوليمرات.
التحليل التوافقي هو قسم من الكيمياء الفراغية الذي يدرس مطابقة الجزيئات ، وتداخلاتها ، واعتماد الخواص الفيزيائية والكيميائية على الخصائص التوافقية. كل شكل محدد يتوافق مع طاقة معينة. في ظل الظروف العادية ، يميل الجزيء إلى الانتقال من الموقع الأقل فائدة من الناحية النشطة إلى الموقع الأكثر فائدة. تسمى الطاقة المطلوبة لتحريك الجزيء من موضع له قيمة دنيا للطاقة الكامنة إلى الموضع المقابل لقيمته القصوى الحاجز المحتمل للدوران.إذا كان مستوى هذه الطاقة مرتفعًا ، فمن الممكن تمامًا عزل الجزيئات ببنية مكانية معينة. مجموعة المطابقات التي تقع بالقرب من الحد الأدنى من الطاقة مع طاقة أقل من حاجز الجهد المقابل هو المطابق. يحدث التغيير في شكل الجزيء الكبير بسبب محدودية دوران الوحدات حول الروابط ، ونتيجة لذلك يأخذ عادةً الشكل الأكثر احتمالًا للملف العشوائي. يمكن أن تؤدي التفاعلات المختلفة داخل الجزيئات وبين الجزيئات إلى عمليات مطابقة مرتبة ، بالإضافة إلى تشكيل كروي مطوي للغاية. من الأهمية بمكان التحليل المطابق في الكيمياء الحيوية. تعتمد الخصائص الكيميائية والبيولوجية للبوليمرات الحيوية إلى حد كبير على خصائصها التوافقية. تعد التغييرات التوافقية جزءًا أساسيًا من جميع العمليات الكيميائية الحيوية تقريبًا. على سبيل المثال ، في التفاعلات الأنزيمية ، يتم تحديد التعرف على الركيزة بواسطة إنزيم من خلال التركيب المكاني وإمكانيات التعديل المطابق المتبادل للجزيئات المشاركة.
المطابقات التالية معروفة:
تشكيل الملف الجزيئي ، أي شكل مطوي إلى حد ما ، والذي يمكن أن يتحمله الملف تحت تأثير الحركة الحرارية ؛
تشكيل عصا صلبة ممدودة (أو قضيب) ؛
تحدث خاصية التشكل اللولبي المميزة للبروتينات والأحماض النووية أيضًا في بوليمرات الفينيل والبولي أوليفينات ، ولكنها لا تستقر بواسطة الروابط الهيدروجينية وبالتالي فهي أقل استقرارًا. يمكن أن يكون اللولب إما أعسر أو يمين ، لأن لا يؤثر على القوة.
التشكل الكروي ، أي جسيم كروي مضغوط للغاية ؛
شكل مطوي ، مميز للعديد من البوليمرات البلورية ؛
التشكل "العمود المرفقي" أو "العمود المرفقي"
كل تشكيل لجزيء كبير له حجم معين. تم إجراء الحساب النظري لحجم الجزيئات الكبيرة لأول مرة لسلسلة مفصلية بحرية ، والتي ، تحت تأثير الحركة الحرارية ، يمكن أن تتحول إلى كرة. يُشار إلى المسافة بين نهايات هذا الملف الجزيئي بالحرف h أو r. من الواضح أنه يمكن أن يختلف من 0 إلى L (طول سلسلة مكشوفة بالكامل). لحساب القيم الوسيطة لـ h ، يتم استخدام جهاز الفيزياء الإحصائية (طرق الميكانيكا الجزيئية) ، نظرًا لوجود عدد كبير جدًا من الروابط في سلسلة واحدة.
يمكن إجراء عملية حسابية مماثلة لسلسلة ذات زوايا رابطة ثابتة ، واستبدالها بسلسلة مفصلية بحرية (سلسلة لا تتفاعل فيها الروابط). في سلسلة مفصلية بحرية ، لا يعتمد موضع كل رابط على موضع الارتباط السابق. في السلسلة الحقيقية ، تكون مواقف الروابط مترابطة. ومع ذلك ، بالنسبة لطول سلسلة كبير جدًا بين روابط بعيدة بدرجة كافية ، يكون التفاعل صغيرًا بشكل مهم. إذا كانت هذه الروابط متصلة بخطوط ، فإن اتجاهات هذه الخطوط تكون مستقلة. هذا يعني أن سلسلة حقيقية تتكون من n وحدات مونومر بطول l يمكن تقسيمها إلى N عناصر إحصائية مستقلة (مقاطع ، مقاطع) بطول A.
يُعتقد أن عنصرًا إحصائيًا ، أو مقطع سلسلة ، بطول A ، لا يعتمد موضعه على موضع الأجزاء المجاورة ، يسمى الجزء الديناميكي الحراريأو مقطع كوهن.
يسمى طول السلسلة المطولة القصوى دون انتهاك زوايا الرابطة محيط شكلطول السلسلة L. وهو مرتبط بطول القطعة من خلال العلاقة
ثالثا. طرق الحساب الكيميائية التجريبية.
للتنبؤ النظري بالتشكيل الأكثر احتمالية للجزيء ، يتم استخدام طريقة الميكانيكا الجزيئية. الميكانيكا الجزيئية هي طريقة حسابية تجريبية لتحديد الخصائص الهندسية وطاقة الجزيئات. يعتمد على افتراض أن طاقة الجزيء يمكن تمثيلها بمجموع المساهمات التي يمكن أن تُعزى إلى أطوال الروابط وزوايا الرابطة وزوايا الالتواء. بالإضافة إلى ذلك ، يوجد دائمًا مصطلح في التعبير العام للطاقة يعكس تفاعل فان دير فالس للذرات غير المقيدة بالتكافؤ ، وهو مصطلح يأخذ في الاعتبار التفاعل الكهروستاتيكي للذرات ويحدد وجود الشحنات الذرية الفعالة.
E \ u003d E sv + E رمح + E torus + E vdv + E بارد
لحساب المصطلحين الأولين ، غالبًا ما يستخدم قانون هوك المعروف من الميكانيكا:
E st \ u003d S k r (r - r 0) 2
من المفترض أن التشكل الأكثر ثباتًا من الناحية الديناميكية الحرارية يتوافق مع الحد الأدنى من الطاقة. تتيح طريقة الميكانيكا الجزيئية الحصول على معلومات للحصول على وصف كامل لهندسة المطابقات المختلفة في الحالة الأرضية.
1.3 التكوين الجزيئي
يتضمن مفهوم التكوين ترتيبًا مكانيًا معينًا لذرات الجزيئات الكبيرة ، والذي لا يتغير أثناء الحركة الحرارية. الانتقال من تكوين إلى آخر مستحيل دون كسر الروابط الكيميائية.
هناك: 1) تكوين ارتباط ، 2) ترتيب قصير المدى - تكوين مرفق الارتباط ، 3) ترتيب بعيد المدى - تكوين أقسام كبيرة (على سبيل المثال ، الكتل وتناوبها ، أو طول الفروع وتوزيعها) ، 5) تكوين سلسلة ممدودة ككل.
تكوين الارتباط. ومن الأمثلة على ذلك تكوينات رابطة الدول المستقلة والتكوينات العابرة لبوليمرات الدين
1.4-cis-polyisoprene 1.4-trans-polyisoprene (المطاط الطبيعي) (gutta-percha) مثال آخر هو l ، d-isomerism. على سبيل المثال،
بالنسبة للبوليمرات التي تحتوي على وحدات CH2 –CHR ~ ، حيث يكون R هو أي جذري ، يكون تكوين اثنين من الأيزومرين ممكنًا: l أعسر ، و d باليد اليمنى
تكوين ارتباط المرفق(وقت قصير). يمكن توصيل الروابط في السلسلة بطريقة وجهاً لوجه وجهاً لوجه:

هو مرفق من الرأس إلى الذيل ، ويتطلب التعلق من الرأس إلى الرأس التغلب على حواجز التنشيط الكبيرة.
بالنسبة للبوليمرات المشتركة ، تزداد أنواع الأيزومرات الهيكلية مقارنة بالبوليمرات المتجانسة. على سبيل المثال ، بالنسبة للبوليمرات المشتركة من البوتادين والستايرين ، فمن الممكن:
1. التناوب المتسلسل للروابط -A-B-A-B-A-B- ،
2. مزيج من الروابط في شكل ثنائيات وثلاثيات–AA – BBB – AA – BBB– ،
3. الجمع الإحصائي للروابط–AA – B – AA – BBB – A – B–. ترتيب التكوين البعيدينتشر على
عشرات ومئات الذرات في السلسلة الرئيسية. على سبيل المثال ، متواليات كبيرة من الكتل في كتلة البوليمرات المشتركة أو متواليات كبيرة من الوحدات التي لها نفس التنظيم الفراغي (على سبيل المثال ، البوليمرات ذات الهياكل متساوية التوضيع ، واللاتينية ، والمتلازمية).
متماثل متماثل متماثل
التكوين العام للدائرةيتم تحديده من خلال الترتيب المتبادل للتسلسلات الكبيرة من الروابط (بترتيب بعيد المدى). على سبيل المثال ، بالنسبة للجزيئات الكبيرة المتفرعة ، يتم عرض أنواع مختلفة من التكوينات في الشكل 4.
أرز. 4. تكوينات الجزيئات الكبيرة

1.4 تشكيل الجزيئات الكبيرة
التشكل هو توزيع متغير في فضاء الذرات أو مجموعات الذرات التي تشكل جزيء ضخم. يمكن أن يحدث الانتقال من شكل إلى آخر بسبب الدوران أو الدوران أو تذبذب الروابط حول الروابط المفردة تحت تأثير الحركة الحرارية أو القوى الخارجية ولا يترافق مع كسر الروابط الكيميائية.
يمكن أن تأخذ البوليمرات تركيبات مختلفة:
تشابك إحصائيهو شكل مطوي. يتشكل عندما تسود شدة الحركة الحرارية الداخلية على التأثير الخارجي. خصائص البوليمرات الخطية [PE ، PP ، PB ، PIB وبوليمرات السلم (بوليفينيل نزيلوكسان).
اللولب - يتكون في البوليمرات بسبب روابط H (على سبيل المثال ، في جزيئات البروتين والأحماض النووية).
الكرة هي جسيم مضغوط جدًا قريب من الشكل الكروي. إنها مميزة للبوليمرات ذات التفاعل الجزيئي القوي (على سبيل المثال ، في PTFE).
قضيب أو خيط موجود في ألكيل بولي أيزوسيانات.
أضعاف التشكل. إنها مميزة للبوليمرات في الحالة البلورية (على سبيل المثال ، في PE).
تشكيل العمود المرفقيأدركت في poly-n-benzamide.
الشكل 5. توافق الجزيئات الكبيرة
1.5 مرونة الجزيئات الكبيرة
تعد المرونة من أهم خصائص البوليمرات ، والتي تحدد الخصائص المرنة للغاية ، والاسترخاء ، والميكانيكية الحرارية للبوليمرات ، فضلاً عن خصائص محاليلها. تميز المرونة قدرة الجزيئات الكبيرة على تغيير شكلها تحت تأثير الحركة الحرارية للوصلات أو التأثيرات الميكانيكية الخارجية. المرونة ناتجة عن الدوران الداخلي للروابط أو أجزاء من الجزيئات الكبيرة بالنسبة لبعضها البعض. ضع في اعتبارك ظاهرة الدوران الداخلي للجزيئات على مثال أبسط مركب عضوي - جزيء الإيثان.
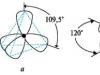
في جزيء الإيثان (CH3 -CH3) ، ترتبط ذرات الكربون بذرات الهيدروجين ومع بعضها بواسطة التساهمية (روابط) ، والزاوية بين اتجاهات روابط σ (زاوية التكافؤ) هي 1090 28 /. يؤدي هذا إلى ترتيب رباعي السطوح للبدائل (ذرات الهيدروجين) في الفضاء في جزيء الإيثان. بسبب الحركة الحرارية في جزيء الإيثان ، تدور مجموعة CH3 بالنسبة إلى الأخرى حول المحور C-C. في هذه الحالة ، يتغير الترتيب المكاني للذرات والطاقة الكامنة للجزيء باستمرار. بيانياً ، يمكن تمثيل الترتيبات المتطرفة المختلفة للذرات في الجزيء على أنها إسقاطات للجزيء على مستوى أفقي (الشكل 6). لنفترض أنه في الموضع a ، الطاقة الكامنة للجزيء هي U1 ، وفي الموضع b تكون U2 ، بينما U1 ≠ U2 ، أي مواقف الجزيء غير متكافئة بقوة. الموضع b ، حيث توجد ذرات H واحدة أسفل الأخرى ، غير مواتية بقوة ، حيث تظهر قوى التنافر بين ذرات H ، والتي تميل إلى نقل الذرات إلى الموضع المناسب بقوة. إذا قبلت
U1 = 0 ، ثم U2 = max.

أرز. 6. صيغ الإسقاط للترتيبات المتطرفة لذرات H في الفضاء في جزيء إيثان.
أرز. 7. اعتماد الطاقة الكامنة للجزيء على زاوية دوران مجموعة الميثيل.
عندما يتم تدوير مجموعة CH3 بالنسبة إلى أخرى بمقدار 600 ، ينتقل الجزيء من الموضع a إلى b ، ثم بعد 600 مرة أخرى إلى الموضع a ، وهكذا. يظهر التغيير في قيم الطاقة الكامنة لجزيء الإيثان من زاوية الدوران φ في الشكل 7. الجزيئات ذات التناظر الأقل (على سبيل المثال ، جزيء ثنائي كلورو الإيثان) لها اعتماد أكثر تعقيدًا U = f (φ).
محتمل (U 0) أو دوران حاجز التنشيط
الأيون هو الطاقة اللازمة لانتقال الجزيء من موضع الحد الأدنى إلى موضع الطاقة الكامنة القصوى. بالنسبة للإيثان ، يكون U0 صغيرًا (U0 = 11.7 كيلوجول / مول) وعند
في درجة الحرارة العادية ، تدور مجموعات CH3 حول الرابطة C-C بسرعة عالية (1010 دورة في الدقيقة).
إذا كان للجزيء احتياطي طاقة أقل من U0 ، فلا يوجد دوران ويحدث فقط تذبذب للذرات بالنسبة إلى موضع الحد الأدنى من الطاقة - وهذا محدود أو
دوران بطيء.
في البوليمرات ، بسبب التفاعلات داخل الجزيئات وبين الجزيئات ، يكون للاعتماد U = f (φ) شكل معقد.
إذا كان أحد مواضع رابط السلسلة يتميز بالطاقة الكامنة U1 ، والآخر - بواسطة U2 ، فإن طاقة الانتقال من موضع إلى آخر تساوي الفرق ∆U = U1 - U2. يميز الفرق بين طاقات الانتقال ∆U من موضع توازن لوحدة جزيء كبير إلى آخر المرونة الديناميكية الحرارية. يحدد قدرة السلسلة على الانحناء تحت تأثير الحركة الحرارية.
سمة أخرى من سمات المرونة هي السرعة التي تنتقل بها الروابط من موضع إلى آخر. يعتمد معدل التحولات التوافقية على نسبة U0 وطاقة التأثيرات الخارجية. كلما زاد عدد U0 ، كلما كان دوران الروابط أبطأ وقلت المرونة. تسمى مرونة الجزيئات الكبيرة ، التي تحددها قيمة U0 مرونة حركية
العوامل التي تحدد مرونة الجزيئات الكبيرة
تتضمن هذه العوامل: قيمة U0 ، البوليمر MM ، كثافة الشبكة المكانية ، حجم البدائل ، ودرجة الحرارة.
حاجز الدوران المحتمل (U 0). تعتمد قيمة U0 على التفاعلات داخل الجزيئات وفيما بينها. دعونا نفكر في العوامل التي تؤثر على U0 ومرونة السلسلة في بوليمرات سلسلة الكربون.
بوليمرات كاربوتشين
في بوليمرات سلسلة الكربون ، الهيدروكربونات المشبعة هي الأقل قطبية. تفاعلاتها داخل الجزيئات وفيما بينها صغيرة ، كما أن قيم U0 و U صغيرة أيضًا ، لذلك تتمتع البوليمرات بمرونة حركية وثرموديناميكية عالية. أمثلة: PE ، PP ، PIB.
قيم U0 منخفضة بشكل خاص بالنسبة للبوليمرات ، حيث يوجد في السلسلة رابطة مزدوجة بجانب الرابطة المفردة.
–CH2 –CH = CH – CH2 - بولي بوتادين
تؤدي المجموعات الكبيرة إلى تفاعلات داخل الجزيئات وفيما بينها. في هذه الحالة ، تؤثر درجة القطبية بشكل كبير
مع إدخال المجموعات القطبية ، هناك ثلاث حالات ممكنة من حيث تأثيرها على المرونة:
1. المجموعات القطبية متقاربة بشكل وثيقوالتفاعلات القوية ممكنة بينهما. يتطلب انتقال هذه البوليمرات من موقع مكاني إلى آخر التغلب على U0 الكبير ، وبالتالي فإن سلاسل هذه البوليمرات هي الأقل مرونة.
2. نادرا ما توجد المجموعات القطبية في السلسلةولا يوجد تفاعل بينهما. قيم U0 و ∆U صغيرة والبوليمرات تتمتع بمرونة حركية وثرموديناميكية عالية.

-CF 2 -CF 2 -
مثال: بولي كلوروبرين
3- يتم ترتيب المجموعات القطبية بحيث يتم تعويض الحقول الكهربائية بشكل متبادل. في هذه الحالة ، فإن إجمالي عزم ثنائي القطب للجزيء الكبير يساوي صفرًا. لذلك ، فإن قيم U0 و U منخفضة ، وتتمتع البوليمرات بمرونة حركية وثرموديناميكية عالية.
مثال: PTFE
بوليمرات Heterochain
في البوليمرات غير المتجانسة ، يكون الدوران ممكنًا حول روابط C-O و C-N و Si-O و C-C. قيم U0 لهذه الروابط صغيرة وتتمتع السلاسل بمرونة حركية كافية. أمثلة: بوليستر ، بولي أميد ، بولي يوريثان ، مطاط السيليكون.
ومع ذلك ، يمكن تقييد مرونة البوليمرات غير المتجانسة من خلال التفاعلات بين الجزيئات بسبب تكوين روابط H (على سبيل المثال ، في السليلوز ، بولي أميدات). السليلوز هو أحد بوليمرات السلسلة الصلبة. يحتوي على عدد كبير من المجموعات القطبية (–OH) وبالتالي التفاعلات داخل الجزيئات وبين الجزيئات والقيم العالية لـ U0 والمرونة المنخفضة هي سمة من سمات السليلوز.
الوزن الجزيئي للبوليمر. تؤدي الزيادة في الوزن الجزيئي للبوليمر إلى زيادة طي السلسلة ، وبالتالي زيادة الجزيئات الكبيرة
تتمتع بمرونة حركية أكبر مقارنة بالجزيئات الكبيرة القصيرة. مع زيادة MM ، يزداد عدد المطابقات التي يمكن أن يعتمدها الجزيء الكبير وتزداد مرونة السلاسل.
كثافة الشبكة المكانية. كلما زادت الروابط الكيميائية بين الجزيئات الكبيرة ، قلت مرونة السلسلة ، أي مع زيادة كثافة الشبكة المكانية ، تقل المرونة. مثال على ذلك هو انخفاض مرونة السلسلة مع زيادة عدد الروابط المتقاطعة في سلسلة الحل.< резитол<резит.
تأثير الحجم وعدد البدائل. تؤدي الزيادة في عدد البدائل القطبية والكبيرة إلى تقليل حركة وحدات الجزيء الكبيرة وتقليل المرونة الحركية. مثال على ذلك هو انخفاض مرونة جزيئات البوليمر المشترك بوتادين - ستيرين مع زيادة في محتوى بدائل فينيل كبيرة الحجم في السلسلة.
إذا كان هناك بدائل في ذرة كربون واحدة في سلسلة البوليمر الرئيسية (على سبيل المثال ، OCH3 و CH3 في وحدات PMMA) ، يصبح الجزيء الضخم صلبًا حركيًا.
درجة حرارة. مع ارتفاع درجة الحرارة ، تزداد الطاقة الحركية للجزيء الكبير. طالما أن قيمة الطاقة الحركية أقل من U0 ، فإن السلاسل تؤدي اهتزازات الالتوائية. عندما تصبح الطاقة الحركية للجزيء الكبير مساوية لـ U0 أو تتجاوزها ، تبدأ الروابط في الدوران. مع زيادة درجة الحرارة ، تتغير قيمة U0 قليلاً ، بينما تزداد سرعة دوران الروابط وتزداد المرونة الحركية.
أسئلة التحكم
1 معلومات عامة عن البوليمرات والمفاهيم والتعاريف.
2 تحديد وإعطاء أمثلة على العناصر العضوية وغير العضوية
البوليمرات العضوية والعضوية.
2 تصنيف بوليمرات homochain ، أمثلة.
3 تصنيف البوليمرات غير المتجانسة ، أمثلة.
4 المرونة الديناميكية الحرارية والحركية للجزيئات الكبيرة. ما هي العوامل التي تؤثر على مرونة الجزيئات؟
5 ما هو تكوين الجزيئات الكبيرة وأنواع التكوينات الممكنة للجزيئات الكبيرة؟ أمثلة.
6 ما هو شكل الجزيئات الكبيرة وأنواع مطابقة الجزيئات الممكنة؟ أمثلة.
7 ما هي المعلمات التي تميز الوزن الجزيئي ،توزيع الوزن الجزيئي والتشتت المتعدد للبوليمرات؟
8 الخصائص الجزيئية للأوليغومرات.
9 تجزئة البوليمرات وبناء المنحنيات الجزيئيةالتوزيع الكتلي الدائري.
تكوين الجزيء غير ذلكالهيكل الأساسي(إنجليزي) - الترتيب المكاني للذرات في. يتم تحديده من خلال قيم زوايا الرابطة وأطوال الروابط المقابلة.
وصف
يتم تحديد تكوين الجزيء الكبير من خلال الترتيب المتبادل لوحدات المونومر المكونة له ، وكذلك من خلال هيكلها. حاليًا ، يستخدم مصطلح "الهيكل" أو "الهيكل الأساسي" عادةً لوصف تكوين الجزيئات الكبيرة.
يتم التمييز بين المدى القصير (تكوين مرفق الوحدات المجاورة) وترتيب التكوين بعيد المدى ، والذي يميز بنية الأقسام الممتدة بشكل كافٍ من الجزيئات الكبيرة. المقياس الكمي للباقة (الترتيب) هو درجة التنظيم الفراغي. بالإضافة إلى ذلك ، يمكن وصف التكتيك بعدد الأنواع المختلفة من أزواج أقرب الجيران (ثنائي ، ثلاثي ، رباعي) ، يتم تحديد توزيعها تجريبيًا. السمة الكمية لتكوين الجزيئات الكبيرة للشبكة الإحصائية ، على سبيل المثال ، هي كثافة الارتباط المتشابك ، أي متوسط قسم السلسلة بين عقد الشبكة.
يتم تحديد تكوين الجزيئات الكبيرة من خلال طرق تحليل حيود الأشعة السينية ، والانكسار ، وما إلى ذلك. كقاعدة عامة ، كل طريقة هي الأكثر "حساسية" لأي خاصية تكوين ؛ وبالتالي ، فإن الرنين المغناطيسي النووي في كثير من الحالات يجعل من الممكن التوصيف الكمي للترتيب التكويني قصير المدى في